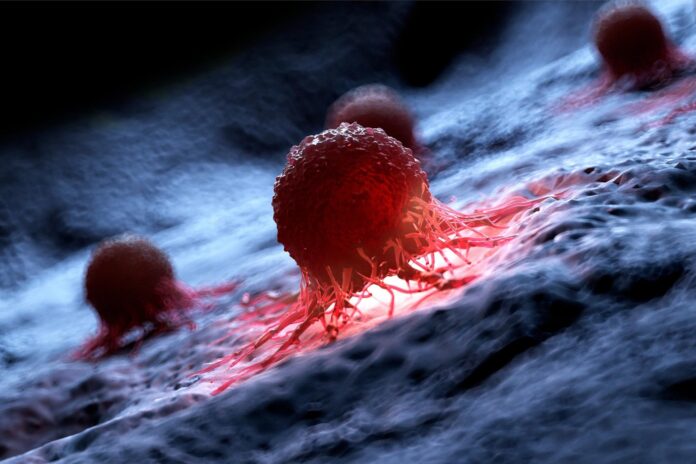
Ein grundlegendes Missverhältnis in der Krebsforschung bremst möglicherweise den medizinischen Fortschritt: Während die Mehrheit der Krebspatienten ältere Erwachsene sind, wird der Großteil der Laborforschung an jungen Probanden durchgeführt. Diese Diskrepanz führt zu einer erheblichen Lücke zwischen erfolgreichen Laborergebnissen und tatsächlichen klinischen Ergebnissen.
Der „Jugendbias“ in der Laborwissenschaft
Die aktuelle Krebsforschung stützt sich stark auf junge Mäuse, die biologisch mit Menschen in ihren frühen Zwanzigern vergleichbar sind. Jüngsten Daten zufolge umfassen weniger als 10 % der Krebsversuche alte Tiere.
Diese Abhängigkeit von „jungen und fitten“ Modellen ist auf praktische Zwänge zurückzuführen:
– Kosten: Jüngere Mäuse sind deutlich günstiger im Unterhalt.
– Zeit: Um das Altern zu untersuchen, müssen Mäuse 18 bis 24 Monate lang gehalten werden, ein langer Zeitraum für viele Forschungszyklen.
– Einfachheit: Junge Mäuse verfügen über ein gesundes, intaktes Immunsystem, das in einer kontrollierten Umgebung leichter zu untersuchen ist.
Diese Voreingenommenheit führt jedoch zu einer „Übersetzungslücke“. Therapien, die in jungen, gesunden Modellen hochwirksam erscheinen, scheitern in klinischen Studien am Menschen oft, weil sie die komplexen biologischen Realitäten älterer Patienten nicht berücksichtigen, die häufig anderen Immunreaktionen und höheren Toxizitätsrisiken ausgesetzt sind.
Neue Erkenntnisse: Der nichtlineare Zusammenhang zwischen Alter und Krebs
Auf der Jahrestagung der American Association for Cancer Research vom Fox Chase Cancer Center vorgestellte Forschungsergebnisse legen nahe, dass die Krebsprogression mit zunehmendem Alter nicht geradlinig verläuft.
In einer Studie zum Thema Melanome entdeckten Forscher ein überraschendes Muster hinsichtlich der Ausbreitung von Krebs:
1. Junge Mäuse: zeigten die geringste Krebsausbreitungsrate.
2. Mäuse mittleren Alters: Die höchsten Raten an Metastasen in lebenswichtigen Organen wie Lunge und Leber.
3. Sehr alte Mäuse: zeigten überraschenderweise einen Rückgang der Krebsausbreitung im Vergleich zur Gruppe mittleren Alters.
Die Rolle von $\gamma\delta$ T-Zellen
Der Schlüssel zu diesem Phänomen scheint in einer bestimmten Gruppe von Immunzellen zu liegen, die als Gamma-Delta-T-Zellen ($\gamma\delta$) bekannt sind. Diese Zellen dienen als früher Abwehrmechanismus gegen Krebs.
Die Studie ergab einen deutlichen Zusammenhang zwischen diesen Zellen und dem Alter:
– Hohe Abwehr: Sowohl junge als auch sehr alte Mäuse hatten einen höheren Spiegel an $\gamma\delta$ T-Zellen, was dazu beitrug, Tumore ruhend oder lokalisiert zu halten.
– Die Schwachstelle im mittleren Alter: Mäuse mittleren Alters hatten deutlich weniger dieser Schutzzellen. Darüber hinaus ergab die Studie, dass Melanomzellen in dieser Altersgruppe aktiv Moleküle freisetzten, die das Immunsystem unterdrücken oder „erschöpfen“ sollten, wodurch sich der Krebs aggressiv ausbreiten konnte.
Die Lücke schließen: Neue Werkzeuge für die Altersforschung
Um dem Mangel an Daten zu älteren Probanden entgegenzuwirken, haben Forscher bei Fox Chase, darunter Mitchell Fane, PhD, und Yash Chabra, PhD, eine spezielle Einrichtung für gealterte Mäuse eingerichtet. Durch die Schaffung etablierter Kolonien älterer Mäuse wollen sie die Kosten- und Zeithürden senken, die Wissenschaftler bisher davon abgehalten haben, das Altern zu untersuchen.
Diese Einrichtung ermöglicht es Forschern, über „Einheitsmodelle“ hinauszugehen und kritische Fragen zu stellen: Warum scheint das Krebsrisiko bei Patienten über 85 zu sinken? Und wie können wir das Immunsystem von Patienten mittleren Alters schützen, um aggressive Metastasen zu verhindern?
„Zu verstehen, wie sich Therapien auf ältere Patienten auswirken, würde uns mehr und bessere Behandlungsmöglichkeiten bieten“, sagt Dr. Mitchell Fane.
Fazit
Durch die Verlagerung des Forschungsschwerpunkts von jungen Modellen auf ältere Probanden können Wissenschaftler besser verstehen, warum sich Krebs im Laufe des Lebens unterschiedlich verhält. Die Auseinandersetzung mit dem „Altersunterschied“ in der Forschung ist von wesentlicher Bedeutung für die Entwicklung personalisierter, wirksamer Behandlungen, die für die tatsächlich am stärksten von der Krankheit betroffene Bevölkerungsgruppe wirken.