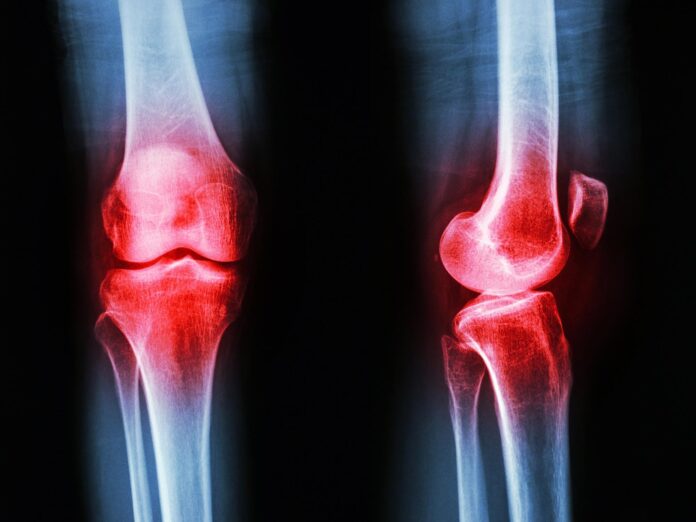
Une étude récente publiée dans la revue Engineering a découvert une nouvelle cible thérapeutique prometteuse pour la polyarthrite rhumatoïde (PR). Les chercheurs ont identifié qu’un composé naturel, l’obakulactone (OL), peut atténuer la maladie non pas en supprimant largement le système immunitaire, mais en corrigeant les déséquilibres métaboliques dans la façon dont le corps traite les graisses.
Changer le paradigme du traitement
Les traitements traditionnels de la polyarthrite rhumatoïde se concentrent souvent sur une large immunosuppression, consistant essentiellement à « réduire » le système immunitaire pour l’empêcher d’attaquer les articulations. Bien qu’efficace, cette approche peut rendre les patients vulnérables aux infections et à d’autres effets secondaires.
Cette nouvelle recherche suggère une alternative plus précise : la régulation métabolique. La polyarthrite rhumatoïde n’est pas seulement un trouble immunitaire ; elle est profondément liée aux perturbations des voies lipidiques (graisses). En ciblant les enzymes qui gèrent ces graisses, les scientifiques pourraient être en mesure de s’attaquer à la cause profonde de l’inflammation plutôt que de simplement gérer les symptômes.
Comment fonctionne l’obakulactone
L’étude s’est concentrée sur l’obakulactone (OL), une molécule dérivée de la plante médicinale traditionnelle Phellodendri cortex. Grâce à une analyse multiomique complexe, les chercheurs ont découvert un mécanisme d’action spécifique :
- Cibler ACOT1 : OL favorise la dégradation d’une protéine spécifique appelée acyl coenzyme A thioestérase 1 (ACOT1).
- Restaurer l’équilibre des acides gras : En décomposant l’ACOT1, l’OL aide à rétablir l’équilibre sain des acides gras insaturés (tels que les acides arachidonique et linoléique) dans le corps.
- Interruption des signaux d’inflammation : Cette correction métabolique perturbe les voies de signalisation clés, en particulier les voies JAK-STAT et PI3K-AKT, connues pour provoquer une inflammation chronique et des cicatrices tissulaires (fibrose).
Preuves issues de modèles expérimentaux
Dans des essais contrôlés impliquant des modèles de rats atteints de polyarthrite rhumatoïde, l’administration d’obakulactone a entraîné des améliorations physiologiques significatives :
- Préservation des articulations : Les sujets traités ont montré une réduction du gonflement des articulations et une meilleure intégrité structurelle du cartilage et du tissu synovial.
- Rééquilibrage immunitaire : OL a réussi à faire passer les cellules immunitaires d’un état « pro-inflammatoire » (macrophages M1) à un état « anti-inflammatoire » (macrophages M2). Cela a également limité la formation de cellules Th17, qui sont les principaux responsables des attaques auto-immunes.
- Réduction des marqueurs inflammatoires : Il y a eu une diminution mesurable des marqueurs sanguins critiques de la PR, notamment IL-6, TNF-α et protéine C-réactive (CRP).
- Contrôle cellulaire : En laboratoire, l’OL a ralenti la croissance agressive des fibroblastes synoviaux (les cellules responsables de l’épaississement douloureux des muqueuses articulaires) et a déclenché leur mort cellulaire programmée pour éviter d’autres dommages.
Pourquoi c’est important
La polyarthrite rhumatoïde touche environ 1 % de la population mondiale, ce qui représente des millions de personnes confrontées à des douleurs chroniques et à un handicap potentiel. Les thérapies actuelles ne parviennent souvent pas à obtenir une rémission complète ou entraînent de lourds effets secondaires.
La découverte qu’un composé naturel peut combler le fossé entre le métabolisme et l’immunologie ouvre une nouvelle porte au développement de médicaments. Si les chercheurs parviennent à développer des versions synthétiques de ce mécanisme, cela pourrait conduire à des thérapies hautement ciblées qui traitent le « carburant » métabolique à l’origine de l’inflammation, offrant potentiellement un soulagement avec moins d’effets secondaires systémiques.
Conclusion
En démontrant que l’obakulactone peut réguler l’homéostasie des acides gras via la protéine ACOT1, cette recherche fournit un modèle pour une nouvelle classe de traitements contre la PR ciblant le dysfonctionnement métabolique pour résoudre l’inflammation chronique.